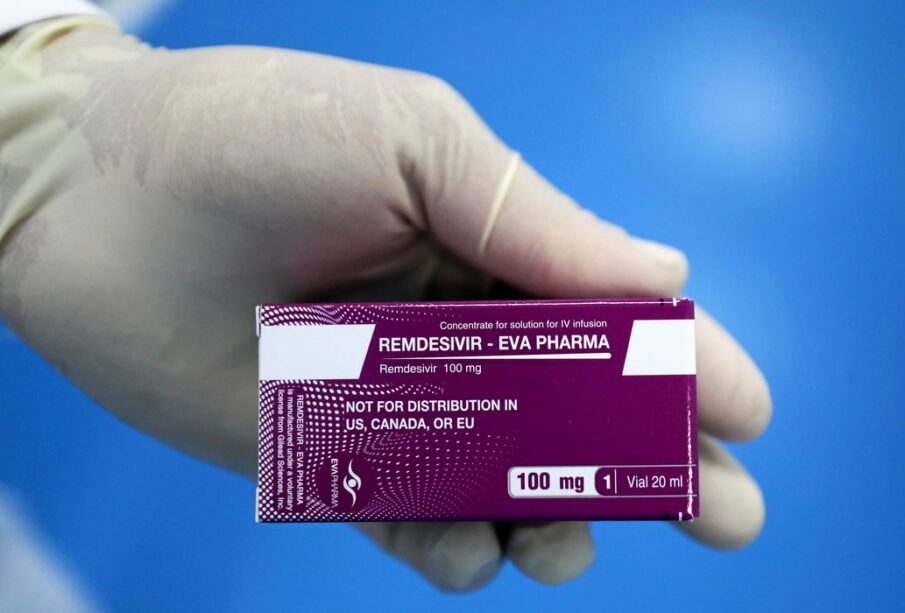
A ANVISA – Agência Nacional de Vigilância Sanitária aprovou dois remédios contra a covid-19. Um deles, o Remdesivir, é para uso pediátrico, injetável e para uso hospitalar; o outro, Paxlovid, é medicamento de uso adulto, com venda sob prescrição médica.
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou a ampliação do uso do medicamento remdesivir, vendido no Brasil pelo nome comercial Veklury, para tratamento pediátrico contra a covid-19.
Agora, o medicamento poderá ser usado por bebês e crianças a partir de 28 dias e peso igual ou superior a 3 kg, que tenham pneumonia e requerem administração suplementar de oxigênio (oxigênio de baixo ou alto fluxo ou outra ventilação não invasiva no início do tratamento).
Crianças pesando 40 kg ou menos, sem necessidade de administração suplementar de oxigênio, mas que apresentam risco aumentado de progredir para covid-19 grave, também poderão fazer o tratamento com o remdesivir.
O produto é um antiviral injetável, de uso hospitalar, produzido no formato de pó para diluição, em frascos de 100 mg, segundo a Anvisa. O antiviral recebeu registro da Anvisa em março de 2021 e, desde então, vem tendo seu uso expandido entre pacientes adultos e adolescentes em casos de covid-19. A substância age impedindo a replicação do coronavírus no organismo, diminuindo o processo de infecção. Cerca de 50 países já autorizam o uso do medicamento.
O outro medicamento aprovado pela ANVISA é o Paxlovid (nirmatrelvir + ritonavir), também utilizado no tratamento da covid-19, para farmácias e hospitais particulares.
A agência autoriza o fornecimento do medicamento para o mercado privado, com a rotulagem e bula em português de Portugal e em espanhol. A agência também aprovou a ampliação da validade do medicamento de 12 meses para 18 meses.
A venda em farmácias deve ser feita sob prescrição médica, com dispensa e orientação pelo farmacêutico ao paciente sobre o uso correto do medicamento. A autorização da Anvisa prevê ainda que o fabricante deve manter e priorizar o abastecimento para o programa do Sistema Único de Saúde (SUS).
Segundo a diretora relatora, Meiruze Freitas, a venda no mercado privado irá aumentar a facilidade de acesso ao tratamento da Covid-19, visto que o remédio deve ser tomado dentro de cinco dias após o início dos sintomas da doença.
SOBRE O REMÉDIO
O Paxlovid, usado no tratamento da covid-19, teve seu uso emergencial aprovado no Brasil em 30 de março deste ano. Composto por comprimidos de nirmatrelvir e ritonavir embalados e administrados juntos, o medicamento é indicado para o tratamento da doença em adultos que não requerem oxigênio suplementar e que apresentam risco aumentado de progressão para covid-19 grave. O medicamento é de uso adulto, com venda sob prescrição médica.
RESTRIÇÕES
Segundo a Anvisa, o Paxlovid não está autorizado para tratamento de pacientes que requerem hospitalização devido a manifestações graves ou críticas da Covid-19. Também não está autorizado para profilaxia pré ou pós-exposição para prevenção da infecção pelo novo coronavírus. O remédio não está autorizado para uso por mais de cinco dias.
Além disso, como não há dados do uso do Paxlovid em mulheres grávidas, recomenda-se que seja evitada a gravidez durante o tratamento com o medicamento e, como medida preventiva, até sete dias após o término do tratamento. O Paxlovid não é recomendado para pacientes com insuficiência renal grave ou com falha renal, uma vez que a dose para essa população ainda não foi estabelecida.
(Com conteúdo da ANVISA)
More News
-
NESTLÉ ABRE INSCRIÇÕES PARA A 3ª FEIRA DE EMPREGABILIDADE
13 de maio de 2024 -
VÍDEO MOSTRA ACONCHEGO AMOROSO EM REENCONTRO DE FILHOTE PERDIDO COM MÃE ELEFANTA
10 de janeiro de 2024






