ANVISA INTERDITA MEDIDOR DE GLICOSE OK PRO APÓS LAUDO INSATISFATÓRIO
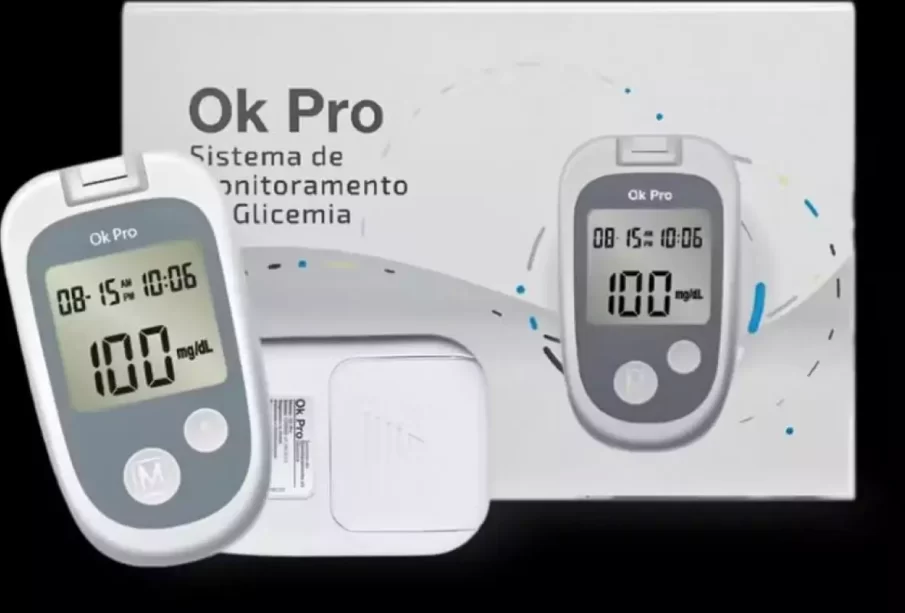
A Agência Nacional de Vigilância Sanitária (Anvisa) determinou, nesta segunda-feira (28), a interdição cautelar do Medidor de Glicose Sanguínea OK PRO. O produto, importado e comercializado pela empresa Biomolecular Technology Comércio, Importação, Exportação e Distribuição de Materiais Médicos e Laboratoriais Ltda., teve sua comercialização e uso suspensos após um laudo laboratorial insatisfatório.
A medida foi estabelecida pela Resolução-RE 2.832, de 25 de julho de 2025, e publicada no Diário Oficial da União. A decisão da Anvisa ocorreu após o recebimento de um laudo de análise do Instituto Nacional de Controle de Qualidade em Saúde (INCQS/Fiocruz). Amostras do medidor de glicose foram reprovadas em testes cruciais, incluindo análise de rotulagem, análise de conformidade, teste de reprodutibilidade e teste de repetibilidade.
A interdição cautelar é uma medida preventiva e temporária que visa impedir a fabricação, comercialização, uso ou funcionamento de um produto ou serviço até que ele esteja em conformidade com as normas estabelecidas e as investigações sejam concluídas.
A Anvisa orienta os usuários do Medidor de Glicose Sanguínea OK PRO a entrarem imediatamente em contato com o Serviço de Atendimento ao Cliente (SAC) do fabricante para obter mais informações, através do e-mail sac@bmtmed.com.br
(Da redação, com informações da ANVISA. Imagem: reprodução)
More News
-
INSCRIÇÕES PARA O SISU DO PRIMEIRO SEMESTRE TERMINAM NA SEXTA-FEIRA
23 de fevereiro de 2023 -
ANVISA MANDA RETIRAR DO MERCADO MARCAS DE SUPLEMENTOS ALIMENTARES
13 de novembro de 2025 -
PIS/PASEP: DATAPREV FAZ REPROCESSAMENTO E DIVULGA NOVA LISTA
16 de março de 2022